2019年底起源于武汉的新冠疫情来势凶猛,传播能力强,至目前以造成7万确诊病例,2千多病人死亡,疫情传播到五大洲26个国家。无数的医生护士、公共卫生人员、科研人员、制药人员和社会各界都为了这场疫情日夜奋斗。抵抗疫情是一个社会各部门高度配合的系统工程,涉及到方方面面。本文主要分析对抗疫情中针对病人群体的关键技术部分。限于篇幅,对轻症病人的支持疗法和针对健康群体的疫苗开发暂不在本文讨论之中。
诊断技术
- 现状
2019新型冠状病毒(中国命名2019-nCoV,国际病毒分类委员会命名SARS-CoV-2,本文统称新冠病毒)引发新型冠状病毒肺炎(WTO官方命名COVID-19) 。这场疫情的扩散一方面是新冠病毒的传播能力强,另一方面是诊断技术不够灵敏,导致许多感染了新冠病毒的病人无法确诊,从而引发更大规模的传染。作为一项诊断技术特别是确诊技术,对灵敏度和特异性要求很高。因为这个季节的流行病毒多以流感病毒为主,突如其来的新冠病毒在序列上容易与流感病毒区分,因此对新冠病毒的诊断特异性容易达到。最重要的是灵敏度,这一指标非常重要,灵敏度不够意味着会造成假阴性,阳性病人得不到确诊,势必影响后面的治疗方案和隔离方案,严重的甚至耽误治疗造成病人不必要的死亡。国家卫健委临床检验中心的专家也给出了原因——目前临床最常用的标本是口咽部拭子和鼻咽部拭子,但某些患者的口咽部或鼻咽部细胞中病毒量较少,导致检测不到病毒核酸。此外,如果标本采集和核酸提取不当,也可能出现“假阴性”的情况。2月12日,中国国家卫计委将临床指标也作为确诊手段,也就是说当前的分子诊断技术未能满足临床需求。虽然并没有太多的数据分析当前诊断试剂盒的指标,我们还是可以从个例中找到一些提示。李文亮医生因公殉职非常可惜,他的微博透露了诊断技术的不足。李文亮医生 1日11日发热到2月1日核酸检测确诊,中间足足隔了20日。之前做了两次核酸检测均为阴性。2月12日美国联邦疾病预防控制中心表示,该中心向各州和至少30个国家发送的一批新冠病毒检测试剂盒已经被证明存在缺陷。
- 提高取样技术的准确性
新冠病毒肺炎的发病部位在下呼吸道,病毒所在的部位主要在肺部。从病人的CT影像也可以看出肺部是病毒浓度高的器官。鼻部取样或者咽部取样容易取不到病毒或者病毒量太少,在后继的分子检测中出现阴性结果。现有的肺镜指导取样在临床上非常繁琐,明显不适合目前的疫情需要。所以简便易操作的肺部取样技术和呼气中病毒浓缩技术会提高样本的质量。设定内参是排除取样不准的一种有效方式。美国疾控中心提供的人源RNase P基因作为核酸提取的内源性参照物,可以减少样本采集及核酸提取质量差导致的假阴性结果。
- 提高灵敏度和特异性
疫情突然,检测试剂盒没有经过严格的临床验证,各个公司生产的试剂盒在灵敏度和特异性这两项指标上参差不齐,一定程度上也是造成新冠病毒诊断假阴性高的原因。对新冠病毒进行多靶点检测可以增加病毒的检出率。严谨的近千例头对头数据显示,思路迪高灵敏度试剂盒最高能多检出40%的真阳性患者,这就意味着每检测1000人就有可能多检出400名新冠病毒感染患者,对“应收尽收,不漏一人”来说意义重大。
- 缩短检测时间
病人数量大,仍然有相当数量的疑似病人等待确诊。缩短检测时间和提高检测效率可以疑似病人等待确诊的时间。除了技术本身的灵敏度和特异性,操作流程简单自动化、大批量、时间短的检测技术也很必要。
目前现有的核酸检测技术大多数采用RT-PCR或者它的改进版,加上病毒核酸准备。往往需要耗时几小时。2月15日,美国麻省理工学院张锋教授课题组绕开了PCR扩增,采用等温扩增技术RPA,检测人员可用量油尺直接读出结果,无需其他复杂仪器,有望在一小时内完成。
药物研发
- 抑制病毒复制
抗病毒药物的研发比抗细菌药物难很多。抗细菌类药物以抗菌素为主,抗菌素属于细菌本身分泌的天然产物,容易获得,而且广谱抗菌素不少。抗病毒类药物主要包括小分子和抗体药物,研制小分子药物和抗体药物的关键在于找到合适的靶点。目前的药物研发策略有两种,一种抑制新冠病毒在人体内的复制,另一种策略是抑制新冠病毒进入人体细胞。现阶段在体外细胞试验中显示抑制病毒活性的的两个候选药物法匹拉韦和瑞德西韦在机理上是抑制病毒复制。法匹拉韦和瑞得西韦都是病毒RNA聚合酶抑制剂/假底物。这两个药物都是前药进入细胞后与病毒类似也是借助宿主细胞内的成分生成代谢产物,然后这些代谢产物在病毒RNA复制时作为核糖核酸原料,被病毒会错误地编入RNA中,当这些假冒核糖核酸积累到一定量之后会导致病毒死亡。在两周前发表的新冠细胞活性实验中,瑞得西韦表现出较高的抑制新冠病毒活性,法匹拉韦抑制新冠活性要弱70倍左右。
冠状病毒的ORF1ab基因编码复制酶多蛋白并在病毒感染中起主要作用。通过RNA干扰技术靶向冠状病毒的ORF1ab基因,是另一种抑制冠状病毒复制的策略。苏州圣诺制药正在运用RNA干扰技术开发新型治疗方法和预防方法,以预防2019新型冠状病毒(2019-nCoV)引起的严重急性呼吸道感染。
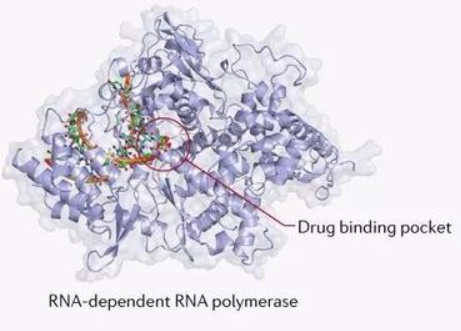
(图1,引自Li & Cllercq,2020)
- 阻断病毒感染细胞
对于抑制病毒进入细胞的策略来说,现阶段公认的较有潜力的靶点是新型冠状病毒的S蛋白和人体宿主身上的病毒受体ACE2(血管紧张素转换酶2)。S蛋白又被称为病毒刺突蛋白,而ACE2则是人体细胞上的一种酶,两者形成“锁与钥匙”的关系。目前已有研究表明新冠病毒可以利用S蛋白识别SARS冠状病毒的受体ACE2入侵人体细胞。因此阻断S蛋白和ACE2的结合理论上推测能够阻止病毒感染人体细胞。主要有三种方式:中和抗体结合病毒S蛋白、阻断屏蔽人体ACE2病毒受体;ACE2融合蛋白(ACE结合结构域与Fc片段融合提高半衰期)与病毒结合。
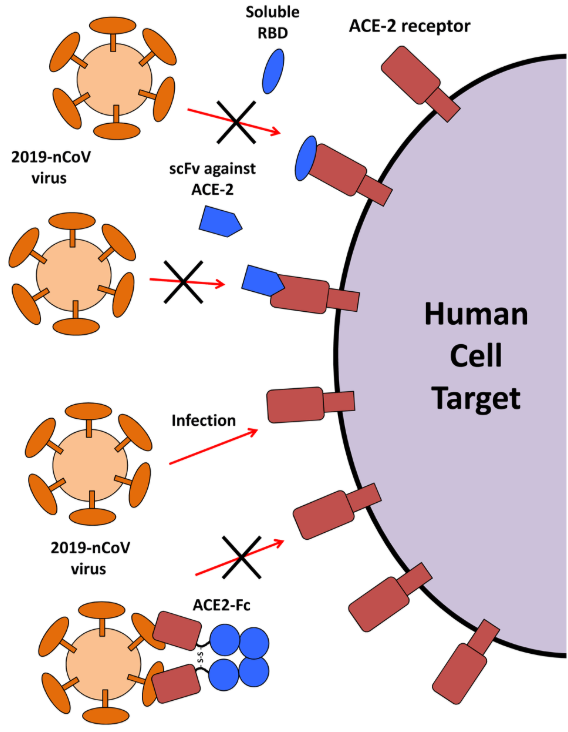
(图2,引自Kruse,2020)
- 旧药新用
鉴于疫情的紧迫性和药物开发的长周期,考虑已上市药物和完成临床一期的候选药物是目前的首选。虽然依然还需要临床试验来验证治疗效果,但至少不需要从临床一期做起。现阶段的选择主要是其它病毒药物,比如法匹拉韦和瑞得西韦,选择余地很小。除此之外,有些不明机制的药物比如氯喹磷酸在体外实验中表现出不错的抑制新冠病毒活性。据报道,临床观察中发现小批量康复病人身上提取的中和抗体具有初步疗效。
报道中的HIV病毒药物落匹那韦/利托那韦在体外实验中对冠状病毒具有非常高的EC50值,预测在临床上不会有很好的疗效。未来若有技术平台比如人工智能药物筛选平台可以快速地匹配旧药与新的适应症,可以理论推测会大大增加候选药物的选择范围。
- 广谱药物
抗病毒药物开发难,广谱抗病毒药物开发更难。因为病毒特别是感染呼吸道的病毒存在不断变异,另外病毒基因组很小,其生命周期的完成依赖宿主提供原料,所以可供选择的靶点非常有限。冠状病毒受体ACE2是存在人体中的靶点,可以不受病毒变异的的影响,靶向ACE2的药物,屏蔽冠状病毒的结合受体或者中和病毒,也许赶不上这次疫情的治疗,但可以用于对抗未来新的冠状病毒感染。
- 重症辅助药物
由2019-nCoV感染引起的死亡主要发生在重症病人中,他们患有或出现严重的呼吸窘迫(ARDS)以及需要机械通气以治疗呼吸衰竭的严重ARDS。由新冠病毒诱导的ARDS的患者死于多器官衰竭。这些进化保守的炎性途径的激活导致炎性细胞因子循环水平的大量增加,从而引起血管渗漏,多个关键器官(肺,肾,心脏,脑,肝,胃肠道)浮肿,并最终导致多器官机能障碍和死亡。预测ARDS相关的生物标记物检测和治疗性药物开发都非常迫切。
总结
早期新冠病毒的急剧爆发与诊断技术的灵敏度低、产量不足、检测耗时长有关。高灵敏高特异操作方面的诊断技术有很大的未满足需求。对于药物研发的策略,从疫情紧迫的角度,老药新用是首选,广谱疫苗和广谱抗病毒药物是未来方向。虽然说呼吸道病毒的毒性会在复制时产生突变而毒性下降,并且可能对高温敏感,现阶段隔离传染源、阻断传播途径依然是最高效的办法。早确诊早干预阻止轻症病人病情加重,以及重症病人提供支持疗法也能有效降低伤亡。
仙瞳资本投研部原创文章,转载请注明出处并添加超链接。
