随着全国医护人员支援湖北陆续到位,医疗资源严重缺乏的局面逐步缓解,中国特别是湖北之外新感染病例的下降,企业逐步开始复工,中国放松对一些城市出行的限制,新冠肺炎(冠状病毒疾病-2019,COVID-19)第一波疫情被控制的趋势明显。但是,第二波疫情大有失控的风险,全球中国之外30多个国家出现新冠肺炎疫情,51人死亡(截止2月26日)。在伊朗、意大利和韩国等国家感染新冠病毒肺炎病例大幅增加后,世界各国对新冠病毒大流行的恐惧增加,2月24日星期一全球股市暴跌,美国股市更是大跌一千点。
难点
机理不清
对于一个新病种,研究清楚其发病机制总是需要时间。新冠病毒(2019-nCoV)作为一个新出现的病原体,其流行病学、进化树、突变频率、病毒分子空间结构、病毒生物学、致病信号通路等知识点是完全新的。近期通过公关卫生、遗传学、结构生物学、分子生物学等各细分领域科研人员的共同科研攻关,取得了阶段性的数据。新冠肺炎在全球的扩散说明新冠病毒的毒性并没有像早期预测的随复制代数增大而下降,新加坡的高发病率也说明新冠病毒并没有像预测那样对高温敏感,新冠病毒与其近亲SARS、MERS相比诱发不同的临床症状。科学研究是一个螺旋上升的过程,完全阐明新冠病毒的特点、侵入人体的机制、重症病人急剧恶化的原因依然需要更大的投入。
靶点稀缺
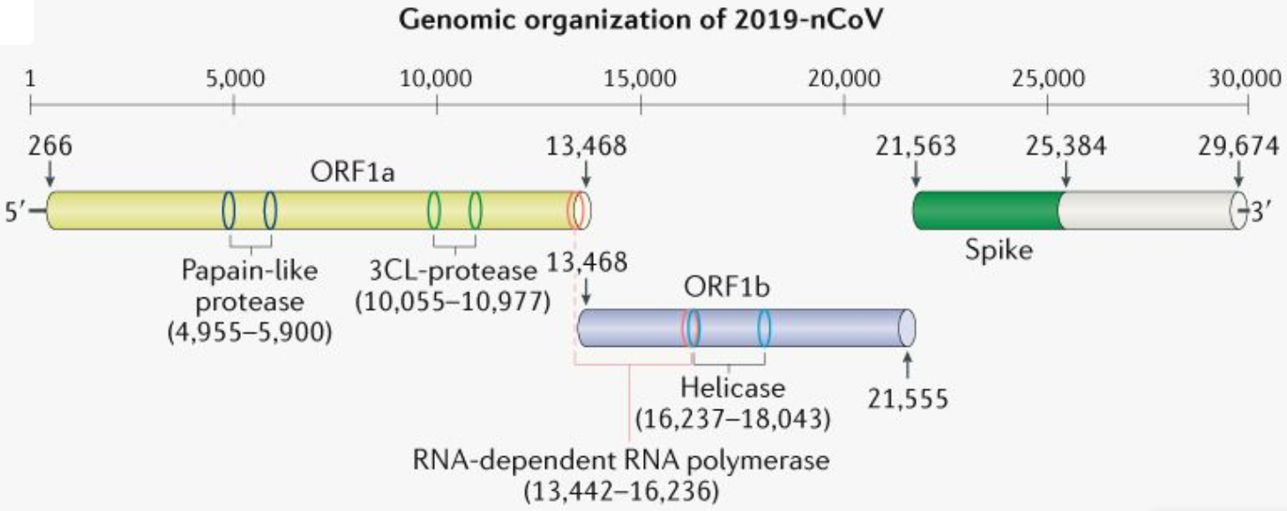
靶点选择的局限是由病毒本身的特点决定的,基因组小且常发生基因突变。CNCB/NGDC建立的2019新型冠状病毒信息库(2019nCoVR)上线运行以来,已汇交并整合全球范围内产出的82株病毒的87条非冗余基因组序列信息,是目前收录2019新型冠状病毒基因组数目最多的数据库。第一批收录的5个新冠病毒全基因组序列也已经在NCBI发布。新冠病毒全长29,889个碱基对(bp),是一种有包膜,正向,单链RNAβ冠状病毒。如下图,相似于SARS和MERS,新冠病毒基因组编码非结构蛋白(例如3-胰凝乳蛋白酶样蛋白酶,木瓜蛋白酶样蛋白酶,解旋酶和RNA依赖性RNA聚合酶),结构蛋白(例如刺突糖蛋白)和辅助蛋白。目前药物研发的靶点主要是RNA依赖性聚合酶、S蛋白和S蛋白结合的人受体ACE2,疫苗研发则主要是通过mRNA表达S蛋白。
对实验室要求高
新冠病毒具有很强的传染性,必须在P3或者P4实验室才能对病毒进行分离、培养以及开展相关后继实验。工作人员也必须经过严格的安全培训,实验动物和材料的后继处理都必须严格按照审定的程序完成。传统的制药企业往往缺乏处理高传染性病毒(特别是通过空气传播)的条件和科研人员。
缺乏动物模型
动物模型是制药的关键一环,可以用于发病机理研究、药物安全性和有效性的初步验证。
中国疾病预防控制中心病毒所检测了585份华南海鲜市场及武汉多家生鲜市场环境标本及动物标本,提示此次疫情可能与野生动物交易有关。中国科学院武汉病毒所通过对新冠病毒基因组序列的比对,也显示出蝙蝠最有可能是新冠病毒的天然宿主。中国动物卫生与流行病学中心的团队检测了4800余份近年来收集的猪、禽、犬、猫等动物样品,可以初步排除新型冠状病毒来源于家禽家畜。华南农业大学团队的研究提出穿山甲可能是新冠病毒的中间宿主之一。目前还不清楚新冠病毒能否感染药物实验中常用的小鼠、大鼠、猴子等动物模型。虽然有些动物模型完成构建的报道,但都没有经过可靠性验证。
临床试验招募病人难
最适合开展临床试验是病人集中的湖北,特别是武汉,但武汉第一线的医护人员连续疲劳作战,当前的任务是抢救病人,要求他们腾出手来开展临床试验有难度。我们知道药物开发是一个金字塔结构,从候选药物的初筛到最终上市是一个逐级递减的过程。因为缺少动物模型,本来在动物模型上可以淘汰的候选药物也推上临床试验,这就造成新冠肺炎临床试验扎堆,据报道多达200多项,良莠不齐,本来就紧张的临床试验资源更加紧缺。
药物市场不确定
目前全世界近8万新冠肺炎确诊病人,主要集中在中国,在中国又集中在武汉。以目前报道的流行病学数据,无法确定最终的病人数量,更无法预测未来几年新冠肺炎的发病人数。对于生物技术公司和药厂来说,药物研发是一个商业行为,虽然有时也有些公益支出。面对一个市场不确定的疾病,加上药物开发的周期长开支大,如果没有特殊的政策支持,生物技术公司和药厂兴趣不大。病人群体不确定,除了导致市场不确定,也造成临床试验难以开展。
药物研发周期长
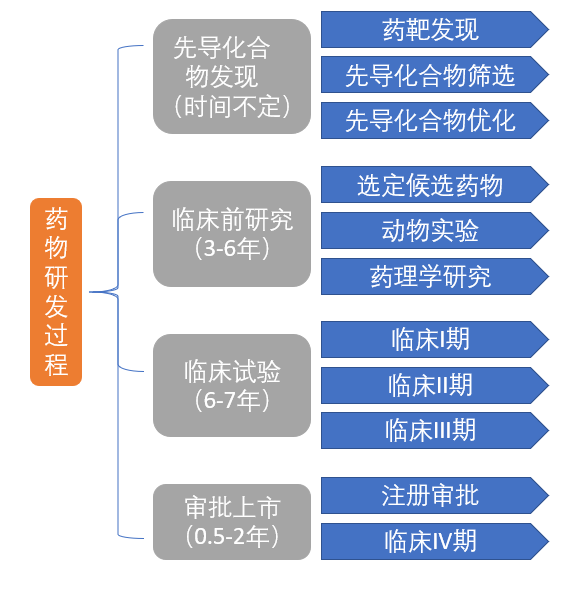
虽然媒体上不时报道有“成功”研发针对新冠肺炎的疫苗和药物,但仔细一读,只是完成疫苗和药物研发的第一步即先导化合物筛选,离最终上市还差十万八千里。疫苗和药物的对新冠肺炎的有效性最终还是需要临床试验数据证明。下图解释了疫苗和药物的研发过程的各个阶段,实验室里设计的疫苗或者初筛的先导化合物,还需要经过临床前研究、临床试验、审批上市三个阶段。除了药物研发的周期长,药物研发的成功率也不高,从临床前到审批上市的平均成功率约10%左右。
对策
药物开发的近期和远期策略
比较明确的是,目前尚无批准用于治疗人类新冠肺炎的药物或疫苗。从技术上说,未来控制或预防新冠肺炎的新发感染可以包括疫苗、单克隆抗体、基于寡核苷酸的疗法、肽、干扰素疗法和小分子药物等。 但是,新的干预措施可能需要数月至数年的开发时间。鉴于新冠肺炎爆发的紧迫性,旧药新用是一种务实救急的近期策略,重点放在重新利用已批准或正在开发的现有抗病毒药物,包括用于治疗HIV、乙肝病毒(HBV)、丙肝病毒(HCV)、流感的药物,特别是抗人冠状病毒比如SARS和MERS的药物。AI药物筛选平台可以扩大旧药的选择范围。
任何药物的研发的都要遵从药物开发的基本规律和流程,如果新冠肺炎像流感一样在全世界传播开来并成为一种每年都有的常见病,稳扎稳打的远期药物开发策略也是必要的。对发病机制的进一步了解、对靶点的深入认识、大规模候选药物的筛选和优化、更优化细胞模型和动物模型的建立、以及逐期开展的临床试验有望研发出针对新冠肺炎的特效药物。通过对新冠病毒和其它冠状病毒更深入的了解,研发出可以抗冠状病毒的广谱药物是更优选择。
疫苗
一般来说,病毒疫苗分为减毒疫苗和灭活疫苗两种。目前对新冠病毒还不了解,制造安全的减毒疫苗和灭活疫苗还需要很长的时间研究,少则数月,多则几年,而且研究和制备时对实验室的安全级别要求高。可以节省时间并对实验室安全级别要求不高的是mRNA疫苗。Moderna公司通过他们的mRNA递送平台,研制了表达新冠病毒S蛋白的mRNA疫苗。从某种程度上模仿了病毒入侵细胞的模式,可能激发人体针对新冠病毒S蛋白的免疫反应。对于mRNA疫苗这种新的疫苗研发策略,虽然在老鼠里成功观察到中和抗体,能否最终成功还是未知数。传统的减毒疫苗和灭活疫苗研发虽然耗时耗力,仍然是必要的。
另外,对新冠病毒突变区域和突变频率的进一步了解,可以提高疫苗研发的成功率。如果能够制备冠状病毒的通用疫苗,未来出现类似疫情,可以马上排上用场。
建立早期评价的动物模型
一窝蜂的将候选药物甚至没有优化的先导化合物跳过动物实验直接推向临床,不仅风险后置,浪费病人资源,而且可能带给受试病人高风险。新冠病毒通过外壳S蛋白结合人肺部的ACE2进入人体,寻找高表达ACE2并与人ACE2高度同源的实验动物种类和建立在肺部高表达人ACE2的动物模型是未来可行的办法。另外的一种可能是,通过病毒溯源,找到新冠病毒真正的中间宿主,在保障安全和政策允许的条件下,将无感染的中间宿主人工养殖成新冠肺炎的实验动物模型。
市场再计算
在新冠肺炎这场疫情中,新冠肺炎病人是直接受害者,更多数量的普通大众是间接受害者。全中国交通管制,国际航班停运、工厂停工、旅游业餐饮业娱乐业停业,学校停课,可以说各行各业都受到影响和损失。据估计,亚洲GDP损失高达1000亿美元。新冠肺炎药物的研发成功,受益不仅是确诊病人,更大的受益是整个社会。如果把药物直接受益与间接受益加在一起,药物的市场将达到万亿人民币。对于影响全社会的疫情,药物的支付当然不能只由病人或者病人的医保方承担,整个间接受益的社会也应该有所付出。
政府、慈善基金与药企合作开发
与其它药物研发不同,政府在新冠肺炎药物研发中的角色非常重要,甚至应该通过财力支持和政策支持成为主要参与者和主导者。2月5日,比尔及梅琳达·盖茨基金会官方宣布,承诺最高捐赠1亿美元,用于加强病例发现、隔离和治疗,保护处于危险中的群体,以及冠状病毒疫苗、治疗方法和诊断方法的研究与开发。2月24日恒大集团宣布将出资1.15亿美元资助广州呼吸健康研究院与美国哈佛大学医学院共同研究新冠病毒的诊断、疫苗、抗病毒药物、以及新冠毒理学,合作期限为5年。这些民间捐助与政府支持相配合,可以激发生物技术和药厂研发新冠肺炎疫苗和新药的积极性。
总结
面对新冠疫情,我们还有很多知识需要深入了解,比如突变频率、致病机理等。鉴于疫情的紧迫性,救急策略以老药新用为主。在中国之外的第二波疫情有失控可能,不排除新冠肺炎在全球流行,稳扎稳打的疫苗和药物研发也是必要的。在政策方面,对于传染性强给社会各行各业带来巨大影响但未来发病群体不明的新冠肺炎,政府在疫苗和药物开发中作用至关重要。政府支持、民间捐助、投资机构、科研机构、生物技术公司、药厂、医疗单位各方的深度合作,期待未来能够成功研发出干预和治疗新冠肺炎的疫苗和药物。
